Expo
ver canal
ver canal
ver canal
ver canal
ver canal
ver canal
ver canal
RadiografíaRM
Medicina NuclearImaginología GeneralTI en ImaginologíaIndustria
Eventos

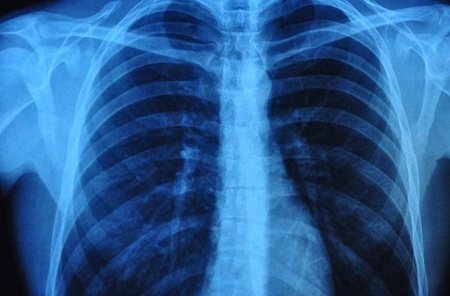
- La IA detecta signos tempranos de envejecimiento a partir de radiografías de tórax
- Avance en rayos X captura tres tipos de contraste de imagen en una sola toma
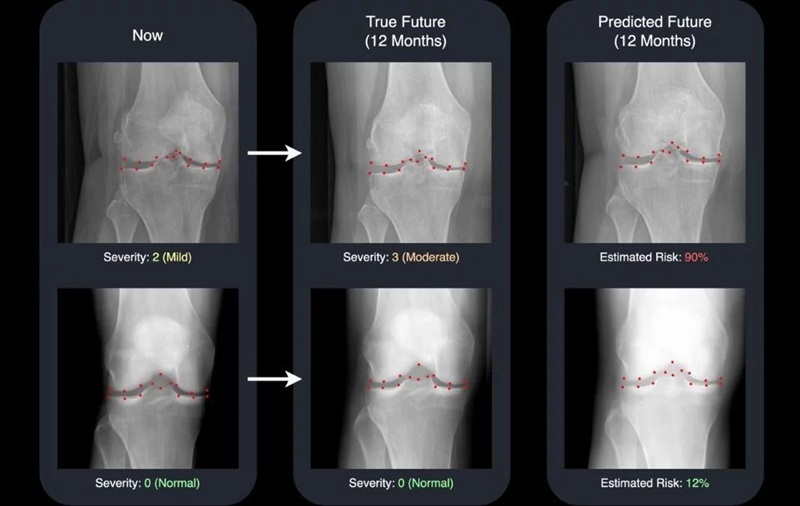
- La IA genera radiografías futuras de rodilla para predecir el riesgo de progresión de la osteoartritis
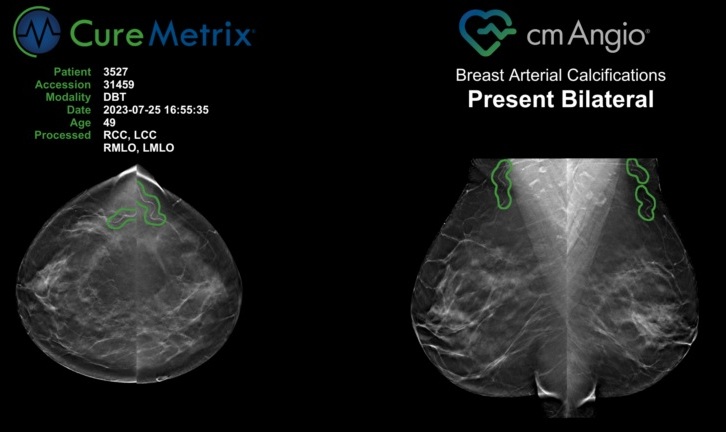
- Algoritmo de IA utiliza mamografías para predecir con precisión el riesgo cardiovascular en mujeres
- Estrategia híbrida con IA mejora la interpretación de mamografías
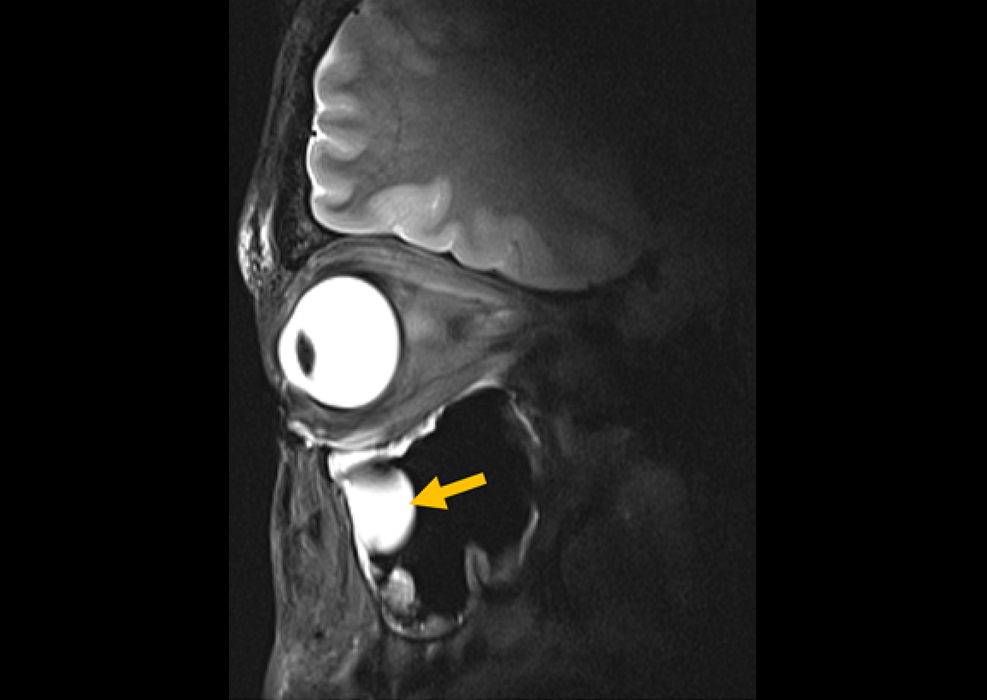
- Modelo de IA analiza y diagnostica resonancias magnéticas cerebrales en segundos
- Avance en resonancia magnética ayuda a evitar pruebas invasivas riesgosas en pacientes cardíacos
- Las RM revelan patrones característicos de actividad cerebral para predecir la recuperación tras una LCT
- Nuevo enfoque de imagen para mejorar el tratamiento de lesiones de la médula espinal
- Modelo asistido por IA mejora las imágenes de resonancia magnética cardíaca
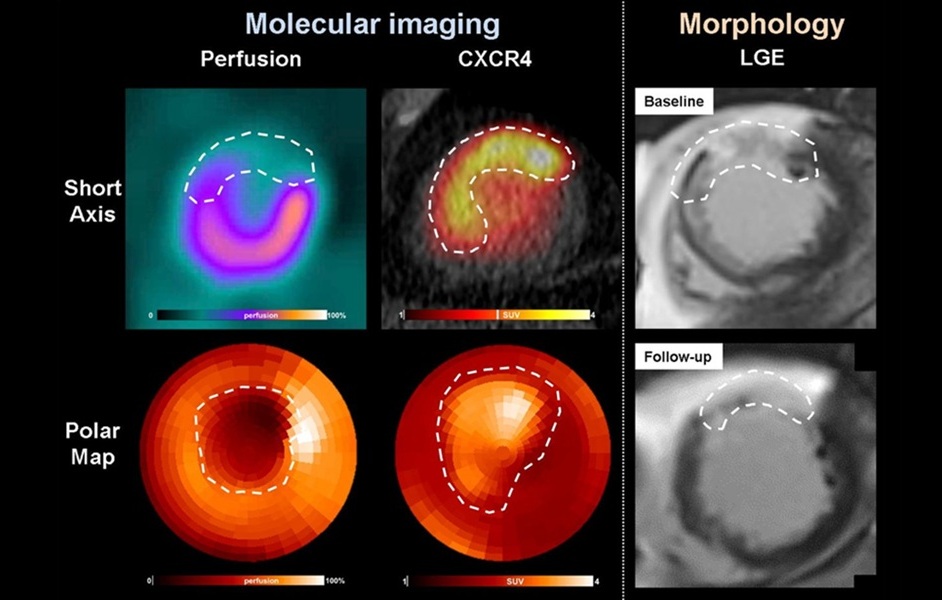
- Las imágenes PET de la inflamación predicen la recuperación y guían la terapia tras un infarto cardíaco
- Un enfoque radioteranóstico detecta, elimina y reprograma cánceres agresivos
- Nueva solución de imagen mejora la supervivencia de los pacientes con cáncer de próstata recurrente
- Nueva cámara permite ver dentro del cuerpo humano para mejorar el escaneo y diagnóstico
- Nueva técnica de PET específica para bacterias detecta infecciones pulmonares difíciles de diagnosticar
- Nueva técnica de imagen produce imágenes 3D en color de tejidos blandos y vasos sanguíneos
- Nuevo sensor portátil de ultrasonido ofrece detección precoz del cáncer de mama
- Escáner de imagen portátil para diagnosticar enfermedades linfáticas en tiempo real
- Sistema de ultrasonido portátil permitirá la monitorización de enfermedades en tiempo real
- Técnica de ultrasonido visualiza vasos sanguíneos profundos en 3D sin agentes de contraste
- Nuevo sistema de imágenes 3D soluciona limitaciones de RM, TC y ultrasonido
- Herramienta basada en IA predice eventos cardiovasculares futuros en pacientes con angina
- Una herramienta basada en IA acelera la detección del cáncer de riñón
- Nuevo algoritmo acelera drásticamente los análisis para la detección del ictus
- Enfoque de escaneo 3D permite una cirugía cerebral ultraprecisa
- Plataforma para el manejo de imágenes agiliza los planes de tratamiento
- Una red global nueva mejora el acceso a la comprensión diagnóstica
- Una estación de trabajo nuevo apoya el flujo de trabajo de la imagenología pensando en los clientes
- Un portal centrado en los pacientes facilita el acceso a la imagenología directa
- Un software de patología digital mejora la eficiencia del flujo de trabajo
- Siemens y Sectra colaboran en la mejora de los flujos de trabajo en radiología
- Bracco Diagnostics y ColoWatch se asocian para ampliar la disponibilidad de pruebas de detección de CCR mediante colonoscopia virtual
- Mindray se asocia con TeleRay para optimizar la entrega de ecografías
- Philips y Medtronic se asocian para el cuidado de accidentes cerebrovasculares
- Siemens y Medtronic forman alianza global para avanzar en tecnologías de imagenología para el cuidado de la columna vertebral

 Expo
Expo
- La IA detecta signos tempranos de envejecimiento a partir de radiografías de tórax
- Avance en rayos X captura tres tipos de contraste de imagen en una sola toma
- La IA genera radiografías futuras de rodilla para predecir el riesgo de progresión de la osteoartritis
- Algoritmo de IA utiliza mamografías para predecir con precisión el riesgo cardiovascular en mujeres
- Estrategia híbrida con IA mejora la interpretación de mamografías
- Modelo de IA analiza y diagnostica resonancias magnéticas cerebrales en segundos
- Avance en resonancia magnética ayuda a evitar pruebas invasivas riesgosas en pacientes cardíacos
- Las RM revelan patrones característicos de actividad cerebral para predecir la recuperación tras una LCT
- Nuevo enfoque de imagen para mejorar el tratamiento de lesiones de la médula espinal
- Modelo asistido por IA mejora las imágenes de resonancia magnética cardíaca
- Las imágenes PET de la inflamación predicen la recuperación y guían la terapia tras un infarto cardíaco
- Un enfoque radioteranóstico detecta, elimina y reprograma cánceres agresivos
- Nueva solución de imagen mejora la supervivencia de los pacientes con cáncer de próstata recurrente
- Nueva cámara permite ver dentro del cuerpo humano para mejorar el escaneo y diagnóstico
- Nueva técnica de PET específica para bacterias detecta infecciones pulmonares difíciles de diagnosticar
- Nueva técnica de imagen produce imágenes 3D en color de tejidos blandos y vasos sanguíneos
- Nuevo sensor portátil de ultrasonido ofrece detección precoz del cáncer de mama
- Escáner de imagen portátil para diagnosticar enfermedades linfáticas en tiempo real
- Sistema de ultrasonido portátil permitirá la monitorización de enfermedades en tiempo real
- Técnica de ultrasonido visualiza vasos sanguíneos profundos en 3D sin agentes de contraste
- Nuevo sistema de imágenes 3D soluciona limitaciones de RM, TC y ultrasonido
- Herramienta basada en IA predice eventos cardiovasculares futuros en pacientes con angina
- Una herramienta basada en IA acelera la detección del cáncer de riñón
- Nuevo algoritmo acelera drásticamente los análisis para la detección del ictus
- Enfoque de escaneo 3D permite una cirugía cerebral ultraprecisa
- Plataforma para el manejo de imágenes agiliza los planes de tratamiento
- Una red global nueva mejora el acceso a la comprensión diagnóstica
- Una estación de trabajo nuevo apoya el flujo de trabajo de la imagenología pensando en los clientes
- Un portal centrado en los pacientes facilita el acceso a la imagenología directa
- Un software de patología digital mejora la eficiencia del flujo de trabajo
- Siemens y Sectra colaboran en la mejora de los flujos de trabajo en radiología
- Bracco Diagnostics y ColoWatch se asocian para ampliar la disponibilidad de pruebas de detección de CCR mediante colonoscopia virtual
- Mindray se asocia con TeleRay para optimizar la entrega de ecografías
- Philips y Medtronic se asocian para el cuidado de accidentes cerebrovasculares
- Siemens y Medtronic forman alianza global para avanzar en tecnologías de imagenología para el cuidado de la columna vertebral

















.jpg)



